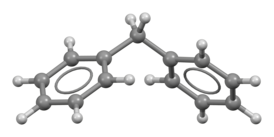
Дифенилметан
| Дифенилметан | |
|---|---|
  | |
| Общие | |
| Хим. формула | C13H12 |
| Физические свойства | |
| Молярная масса | 168.234 г/моль |
| Плотность | 1.006 г/см³ |
| Энергия ионизации | 8,55 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | 22-24 °C |
| • кипения | 264 °C |
| Классификация | |
| Рег. номер CAS | 101-81-5 |
| PubChem | 7580 |
Рег. номер EINECS |
202-978-6 |
| SMILES | |
| InChI | |
| ChEBI | 38884 |
| ChemSpider | 7299 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дифенилметан — органическое соединение класса
Физические и химические свойства
Дифенилметан представляет собой бесцветные прозрачные кристаллы с запахом герани, нерастворимые в воде, но хорошо растворяющиеся в органических растворителях (
Дифенилметан благодаря наличию метиленовой группы и бензольных колец обладает свойствами как алифатических, так и ароматических соединений: атомы водорода в метиленовой группе способны замещаться на атомы галогена, нитрогруппу или другие функциональные группы:
окисляться до карбонильной группы с образованием
Дегидрирование дифенилметана над платиновым катализатором приводит к флуорену, гидрирование над никелем — к дициклогексилметану.
Бензольные кольца молекулы дифенилметана вступают в реакции
Методы синтеза
- Из бензилхлорида и бензола в присутствии хлорида алюминия[2]:
- Из бензола и дихлорметана в присутствии хлорида алюминия:
Существует также способ синтеза дифенилметана из бензола и формальдегида в среде 85%-ной серной кислоты.
Применение
Дифенилметан используется как
Примечания
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ W. W. Hartman and Ross Phillips (1943). «Diphenylmethane». Org. Synth.; Coll. Vol. 2: 232.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2 (Даф-Мед). — 671 с. — ISBN 5-82270-035-5.
Для улучшения этой статьи желательно:
|
![{\displaystyle {\mathsf {(C_{6}H_{5})_{2}CH_{2}{\xrightarrow[{170^{o}t}]{PCl_{5}}}(C_{6}H_{5})_{2}CCl_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4bf33985498a2b2cd2c23e9699c795152f59b433)
![{\displaystyle {\mathsf {(C_{6}H_{5})_{2}CH_{2}{\xrightarrow[{}]{H_{2}CrO_{4}}}+(C_{6}H_{5})_{2}CO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/682045d9d45bddb44de66a23afd7983bc6f891b1)
![{\displaystyle {\mathsf {C_{6}H_{5}CH_{2}Cl+C_{6}H_{6}{\xrightarrow[{}]{AlCl_{3}}}(C_{6}H_{5})_{2}CH_{2}+HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/db995b182d573007edd09b3b983460f1fec2c412)
![{\displaystyle {\mathsf {CH_{2}Cl_{2}+2C_{6}H_{6}{\xrightarrow[{}]{AlCl_{3}}}(C_{6}H_{5})_{2}CH_{2}+2HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d4bc1952a5dffebad0e1f6810671d30c21d36732)