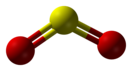
Оксид серы(IV)
| Оксид серы(IV) | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Оксид серы(IV) | ||
| Хим. формула | SO2 | ||
| Рац. формула | SO2 | ||
| Физические свойства | |||
| Состояние | бесцветный газ | ||
| Молярная масса | 64,054 г/моль | ||
| Плотность | 0,002927 г/см³ | ||
| Энергия ионизации | 12,3 ± 0,1 эВ[6] и 12,32 эВ[7] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −75,5 °C | ||
| • кипения | −10,01 °C | ||
| Тройная точка | 197,69 К (—75,46 °C), 0,0157 МПа[1] | ||
| Критическая точка | 430,7 (157,55 °C), 7,88 МПа, 122 см3/моль[2] | ||
| Энтальпия | |||
| • образования | —296,90[3][4]; —297,05[5] кДж/моль | ||
| Давление пара | 3,2 ± 0,1 атм[6] | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 11,5 г/100 мл | ||
| Структура | |||
| Дипольный момент | 5,4E−30 Кл·м[7] | ||
| Классификация | |||
| Рег. номер CAS | [7446-09-5] | ||
| PubChem | 1119 | ||
Рег. номер EINECS |
231-195-2 | ||
| SMILES | |||
| InChI | |||
| Кодекс Алиментариус | E220 | ||
| RTECS | WS4550000 | ||
| ChEBI | 18422 | ||
| ChemSpider | 1087 | ||
| Безопасность | |||
| Предельная концентрация | 10 мг/м³ | ||
| Токсичность | Класс опасности III | ||
| Пиктограммы ECB |
|
||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Окси́д се́ры(IV) (диокси́д се́ры, двуокись серы, серни́стый газ, серни́стый ангидри́д) — соединение серы с кислородом состава SO2. В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички). В высоких концентрациях токсичен. Под давлением сжижается при комнатной температуре. Растворяется в воде с образованием нестойкой серни́стой кислоты; растворимость 11,5 г/100 г воды при 20 °C, снижается с ростом температуры. Растворяется также в этаноле и се́рной кислоте. Один из основных компонентов вулканических газов. Зарегистрирован в качестве пищевой добавки с номером E220.
Получение
Промышленный способ получения — сжигание серы или обжиг
В лабораторных условиях и в природе SO2 получают воздействием сильных кислот на сульфиты и гидросульфиты. Образующаяся сернистая кислота H2SO3 сразу разлагается на SO2 и H2O:
Химические свойства

Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима):
С щелочами образует сульфиты:
Химическая активность SO2 весьма велика. Наиболее ярко выражены
Предпоследняя реакция является качественной реакцией на сульфит-ион SO32− и на SO2 (обесцвечивание фиолетового раствора).
В присутствии сильных восстановителей SO2 способен проявлять
Или для получения фосфорноватистой кислоты:
Применение
Большая часть оксида серы(IV) используется для производства сернистой кислоты. Используется также в виноделии в качестве консерванта (пищевая добавка E220). Газ убивает микроорганизмы, поэтому им окуривают овощехранилища и склады. Оксид серы(IV) используется для отбеливания соломы, шёлка и шерсти, то есть материалов, которые нельзя отбеливать хлором. Применяется он также и в качестве растворителя в лабораториях[8]. Оксид серы(IV) применяется также для получения различных солей сернистой кислоты.
Токсичность и безопасность
Оксид серы(IV) SO2 в высоких дозах очень токсичен. Симптомы при отравлении сернистым газом — насморк, кашель, охриплость, сильное першение в горле и своеобразный привкус. При вдыхании сернистого газа более высокой концентрации — удушье, расстройство речи, затруднение глотания, рвота, возможен острый отёк лёгких.
При кратковременном вдыхании оказывает сильное раздражающее действие, вызывает кашель и першение в горле.
- в атмосферном воздухе максимально разовая — 0,5 мг/м³, среднесуточная — 0,05 мг/м³;
- в помещении (рабочая зона) — 10 мг/м³.
По степени воздействия на человеческий организм сернистый ангидрид относится к III классу опасности («умеренно-опасное химическое вещество») согласно ГОСТ 12.1.007-76.
Интересно, что чувствительность по отношению к SO2 весьма различна у отдельных людей, животных и растений. Так, среди растений наиболее устойчивы по отношению к сернистому газу берёза и дуб, наименее — роза, сосна и ель.
По данным исследования[9] средний порог восприятия запаха может превышать ПДК (21 мг/м3), а у части людей порог был значительно выше среднего значения.
В качестве пищевой добавки оксид серы признан безопасным для потребления, однако у астматиков он может вызвать аллергические реакции
Биологическая роль
Роль эндогенного
Показано, что эндогенный сернистый газ играет роль в предотвращении повреждения лёгких, уменьшает образование свободных радикалов, оксидативный стресс и
Считают, что эндогенный сернистый газ играет важную физиологическую роль в регуляции функций сердечно-сосудистой системы, а нарушения в его метаболизме могут играть важную роль в развитии таких патологических состояний, как лёгочная гипертензия, гипертоническая болезнь, атеросклероз сосудов, ишемическая болезнь сердца, ишемия-реперфузия и др.[15].
Показано, что у детей с врождёнными пороками сердца и лёгочной гипертензией повышен уровень гомоцистеина (вредного токсичного метаболита цистеина) и снижен уровень эндогенного сернистого газа, причём степень повышения уровня гомоцистеина и степень снижения выработки эндогенного сернистого газа коррелировала со степенью выраженности лёгочной гипертензии. Предложено использовать гомоцистеин как маркер степени тяжести состояния этих больных и указано, что метаболизм эндогенного сернистого газа может быть важной терапевтической мишенью у этих больных[16].
Также показано, что эндогенный сернистый газ понижает пролиферативную активность клеток
Эндогенный сернистый газ оказывает эндотелий-зависимое
Эндогенный сернистый газ также уменьшает повреждение миокарда, вызванное экспериментальной гиперстимуляцией
Воздействие на атмосферу
Из-за образования в больших количествах в качестве отходов диоксид серы является одним из основных газов, загрязняющих атмосферу.
Наибольшую опасность представляет собой загрязнение соединениями серы, которые выбрасываются в атмосферу при сжигании угольного топлива, нефти и природного газа, а также при выплавке металлов и производстве серной кислоты.
Антропогенное загрязнение серой в два раза превосходит природное
Необходимо отметить также, что диоксид серы имеет максимум в спектре поглощения света в ультрафиолетовой области (190—220 нм), что совпадает с максимумом в спектре поглощения озона. Это свойство диоксида серы позволяет утверждать, что наличие этого газа в атмосфере имеет также положительный эффект, предотвращая возникновение и развитие онкологических заболеваний кожи человека. Диоксид серы в атмосфере Земли существенно ослабляет влияние парниковых газов (диоксид углерода, метан) на рост температуры атмосферы[22].
Наибольших концентраций сернистый газ достигает в северном полушарии, особенно над территорией США, Европы, Китая, европейской части России и Украины. В южном полушарии содержание его значительно ниже[23].
Примечания
- ↑ Фёдоров П. И., Тройная точка, 1998, с. 12.
- ↑ Хазанова Н. Е., Критическое состояние, 1990, с. 543.
- ↑ Карапетьянц М. Х.,, Дракин С. И., Общая и неорганическая химия, 2000, с. 181.
- ↑ Стандартные энтальпии образования, стандартные энергии Гиббса образования неорганических веществ и их стандартные энтропии при 298,15 К. Дата обращения: 22 декабря 2020. Архивировано 27 июля 2020 года.
- ↑ Киреев В. А., Краткий курс физической химии, 1978, с. 179.
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0575.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Гордон А., Форд Р. Спутник химика / Пер. на русск. Е. Л. Розенберга, С. И. Коппель. — М.: Мир, 1976. — 544 с.
- 9 ноября 2019 года.
- ↑ .
- ↑ World Health Organization. SULFUR DIOXIDE // Joint FAO/WHO Expert Committee on Food Additives. Архивировано 15 октября 2022 года.
- ↑ CFR - Code of Federal Regulations Title 21 (англ.). FDA. Дата обращения: 16 октября 2022. Архивировано 17 октября 2022 года.
- ↑ Liu, D.; Jin, H; Tang, C; Du, J. Sulfur dioxide: a novel gaseous signal in the regulation of cardiovascular functions (англ.) // Mini-Reviews in Medicinal Chemistry[англ.] : journal. — 2010. — Vol. 10, no. 11. — P. 1039—1045. — PMID 20540708. Архивировано 26 апреля 2013 года.
- 21 сентября 2016 года.
- ↑ Tian H. Advances in the study on endogenous sulfur dioxide in the cardiovascular system. // Chin Med J. — Nov 2014. — Т. 127, вып. 127(21), № 21. — С. 3803—3807. — PMID 25382339. Архивировано 8 ноября 2016 года.
- ↑ Yang R, Yang Y, Dong X, Wu X, Wei Y. Correlation between endogenous sulfur dioxide and homocysteine in children with pulmonary arterial hypertension associated with congenital heart disease (кит.) // Zhonghua Er Ke Za Zhi. — Aug 2014. — 第52卷, 第52(8)期, 第8数. — 第625—629 页. — PMID 25224243.
- .
- 9 мая 2017 года.
- .
- ↑ Серный ангидрид, его воздействие на окружающую среду. Дата обращения: 21 ноября 2013. Архивировано 23 ноября 2014 года.
- ↑ Основы расчета нормативов пдв. Дата обращения: 21 ноября 2013. Архивировано 20 апреля 2015 года.
- ↑ Проблемы загрязнения атмосферы. Парниковый эффект. Дата обращения: 21 ноября 2013. Архивировано 3 декабря 2013 года.
- ↑ Экологические кризисы. Дата обращения: 21 ноября 2013. Архивировано 10 июня 2015 года.
Литература
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. — 4-е изд., стер. — М.: Химия, 2000. — 592 с.
- Киреев В. А. Краткий курс физической химии. — 5-е изд., стер. — М.: Химия, 1978. — 621 с.
- Фёдоров П. И. Тройная точка // Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — С. 12.
- Хазанова Н. Е. Критическое состояние // Советская энциклопедия, 1990. — Т. 2: Даф — Мед. — С. 541—543.
Ссылки
- Global map of sulfur dioxide distribution Архивная копия от 8 февраля 2017 на Wayback Machine (англ.)
- United States Environmental Protection Agency Sulfur Dioxide page Архивная копия от 25 декабря 2008 на Wayback Machine (англ.)
- International Chemical Safety Card 0074 Архивная копия от 7 августа 2019 на Wayback Machine (англ.)
- IARC Monographs. «Sulfur Dioxide and some Sulfites, Bisulfites and Metabisulfites» v54. 1992. p131. (англ.)
- Sulfur Dioxide, Molecule of the Month Архивная копия от 3 августа 2019 на Wayback Machine (англ.)









![{\displaystyle {\mathsf {2SO_{2}+O_{2}{\xrightarrow[{Pt}]{450^{o}C}}2SO_{3}}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eb2802a01539be827b772f6db4a2f3fb78ef3c80)




