Тройная точка


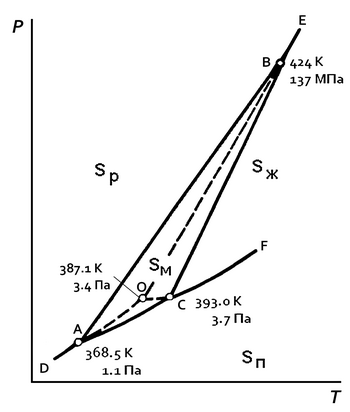
Sp — ромбическая сера; Sм — моноклинная сера; Sж — жидкая сера; Sп — пары серы


Тройна́я то́чка в
Если для индивидуального вещества существует тройная точка, соответствующая состоянию, в котором равновесные фазы находятся в различных агрегатных состояниях (твёрдом, жидком и газообразном), то она единственна[10][11], и её называют основной тройной точкой[12][13][14] или фундаментальной точкой[15]. Основная тройная точка не существует для гелия[16].
Поскольку координаты тройной точки задаются значениями P и T и не зависят от V, то на трёхмерной фазовой диаграмме P—T—V и её проекции на плоскость P—V равновесным состояниям трёх фаз соответствует тройная линия (triple line)[17][18].
В основной тройной точке сходятся три
Единственность и нонвариантность основной тройной точки позволяет использовать её как репер температуры. В частности, температурная шкала Кельвина использует тройную точку воды в качестве опорной.
Правило фаз Гиббса ограничивает число сосуществующих фаз — однокомпонентная система в равновесии не может иметь больше трёх фаз[1][2], — но не накладывает ограничений на их агрегатное состояние. Поэтому в случае энантиотропии на диаграмме состояния помимо основной тройной точки появляются дополнительные тройные точки, отвечающие:
- равновесию двух твёрдых фаз с жидкостью (например, аллотропных модификаций кристаллической серы — ромбической и моноклинной — и жидкой серы);
- равновесию двух твёрдых фаз с паром;
- равновесию трёх твёрдых фаз.
Возможно также появление метастабильных тройных точек, расположенных на пересечении линий метастабильных двухфазных равновесий (или продолжений этих линий). В случае монотропии появляется только метастабильная тройная точка[3].
Кристаллическая элементарная сера диморфна, поэтому на фазовой диаграмме серы (см. рисунок; для давления использован логарифмический масштаб) имеются три стабильные тройные точки и одна метастабильная, каждая из которых отвечает условиям термодинамического равновесия трёх фаз[21]:
- точка А (дополнительная): равновесие твёрдой ромбической Sp, твёрдой моноклинной Sм и газообразной серы Sп;
- точка В (дополнительная): равновесие твёрдой ромбической, твёрдой моноклинной и жидкой серы Sж;
- точка С (основная): равновесие твёрдой моноклинной, расплавленной и газообразной серы;
- точка О (метастабильная): метастабильное равновесие между перегретой твёрдой ромбической, переохлаждённой жидкой и газообразной серой.
Как показывает фазовая диаграмма, ромбическая сера не может одновременно находиться в равновесии с расплавом и парами серы[22], поэтому в основной тройной точке твёрдая фаза представлена моноклинной серой. Метастабильная тройная точка появляется вследствие низкой скорости превращения одной кристаллической модификации серы в другую[23].
В дополнительных тройных точках гелия сосуществуют либо две жидкие фазы (Не I и Не II) и кристаллический гелий, либо две жидкие фазы и газообразный гелий[24]. Для воды в 1975 г. были известны семь дополнительных тройных точек, из них три — для трёх твёрдых фаз[25]. Современные данные см. в статье Фазовая диаграмма воды и на приведённой в этой статье диаграмме.
При увеличении числа компонентов системы (раствора или сплава) увеличивается и число независимых параметров, характеризующих эту систему. Для описания
В
Параметры тройной точки некоторых веществ
Параметры тройной точки некоторых веществ приведены в таблице[29][30].
| Вещество | Фазы | Температура, °С | Давление, МПа |
|---|---|---|---|
| Ar (аргон) | твёрдая—жидкая—газовая | —189,34 | 0,0689 |
| Br2 (бром) | твёрдая—жидкая—газовая | —7,25 | 0,0046548 |
| С (углерод) | графит—алмаз—жидкость | 3700 | 11000 |
| Cl2 (хлор) | твёрдая—жидкая—газовая | —101,05 | 0,001354 |
| F2 (фтор) | твёрдая—жидкая—газовая | —219,61 | 0,00019198 |
| H2 (водород) | твёрдая—жидкая—газовая | —259.19 | 0,007205 |
| Kr (криптон) | твёрдая—жидкая—газовая | —157,22 | 0,073 |
| N2 (азот) | твёрдая—жидкая—газовая | —210,01 | 0,012520 |
| Ne (неон) | твёрдая—жидкая—газовая | —248,61 | 0,043265 |
| Rn (радон) | твёрдая—жидкая—газовая | —71 | 0,07 |
| Ti (титан) | 640 ± 50 | (8 ± 0,7)•1000 | |
| Tl (таллий) | α—β—γ | 115 | 3900 |
| Xe (ксенон) | твёрдая—жидкая—газовая | —111,63 | 0,08 |
См. также
Примечания
- ↑ 1 2 3 Физическая энциклопедия. Тройная точка. Дата обращения: 19 апреля 2015. Архивировано из оригинала 21 апреля 2017 года.
- ↑ 1 2 Большая Советская Энциклопедия. Тройная точка. Дата обращения: 19 апреля 2015. Архивировано из оригинала 6 июня 2017 года.
- ↑ 1 2 3 4 Химическая энциклопедия, т. 5, 1998, с. 12.
- ↑ 1 2 Мюнстер А., Химическая термодинамика, 1971, с. 151.
- ↑ Хачкурузов Г. А., Основы общей и химической термодинамики, 1979, с. 132.
- ↑ 1 2 IUPAC Gold Book, 2014, p. 1567.
- ↑ Мейер К., Физико-химическая кристаллография, 1972, с. 133—134.
- ↑ Булидорова Г. В. и др., Физическая химия, 2012, с. 228.
- ↑ Иванова Т. Е., Химическая термодинамика и ее применение в нефтегазовом деле, 2014, с. 87.
- ↑ Жданов Л. С., Жданов Г. Л., Физика, 1984, с. 119.
- ↑ Мякишев Г. Я., Синяков А. З., Физика. Молекулярная физика. Термодинамика, 2010, с. 310.
- ↑ Термодинамика. Основные понятия. Терминология. Буквенные обозначения величин, 1984, с. 22.
- ↑ Новиков И. И., Термодинамика, 1984, с. 215.
- ↑ Романюк В. Н. и др., Лабораторные работы (практикум) по дисциплине «Техническая термодинамика», ч. 2, 2003, с. 21.
- ↑ Леонова В. Ф., Термодинамика, 1968, с. 144.
- ↑ 1 2 Глаголев К. В., Морозов А. Н., Физическая термодинамика, 2007, с. 241.
- ↑ Хейвуд Р., Термодинамика равновесных процессов, 1983, с. 99.
- ↑ Техническая термодинамика. Под ред. Э. И. Гуйго, 1984, с. 146.
- ↑ Мюнстер А., Химическая термодинамика, 1971, с. 222.
- ↑ 1 2 Жданов Л. С., Жданов Г. Л., Физика, 1984, с. 121.
- ↑ Булидорова Г. В. и др., Физическая химия, 2012, с. 228.
- ↑ Ансельм А. И., Основы статистической физики и термодинамики, 1973, с. 227.
- ↑ Мейер К., Физико-химическая кристаллография, 1972, с. 134.
- ↑ Глаголев К. В., Морозов А. Н., Физическая термодинамика, 2007, с. 242.
- ↑ Эйзенберг Д., Кауцман В., Структура и свойства воды, 1975, с. 95—96.
- ↑ Раковский А. В., Курс физической химии, 1939, с. 276.
- ↑ Еремин Е. Н., Основы химической термодинамики, 1978, с. 329.
- ↑ Бобкова Н. М., Физическая химия тугоплавких материалов, 2007, с. 103.
- ↑ Дриц М. Е. и др., Свойства элементов, 1985.
- ↑ Фёдоров П. И., Тройная точка, 1998, с. 12.
Литература
- Nic M., Jirat J., Kosata B., Jenkins A. IUPAC Compendium of Chemical Terminology (Gold Book) (англ.). — 2.3.3. — International Union of Pure and Applied Chemistry, 2014. — 1622 p. — ISBN 0-9678550-9-8.
- Ансельм А. И. Основы статистической физики и термодинамики. — М.: Наука, 1973. — 424 с.
- Бобкова Н. М. Физическая химия тугоплавких неметаллических и силикатных материалов. — Минск: Вышэйшая школа, 2007. — 303 с. — ISBN 978-985-06-1389-9.
- Булидорова Г. В., Галяметдинов Ю. Г., Ярошевская Х. М., Барабанов В. П. Физическая химия. — Казань: Изд-во Казан. нац. исслед. технол. ун-та, 2012. — 396 с. — ISBN 978-5-7882-1367-5.
- Глаголев К. В., Морозов А. Н. Физическая термодинамика. — 2-е изд., испр. — М.: Изд-во МГТУ им. Н. Э. Баумана, 2007. — 270 с. — (Физика в техническом университете). — ISBN 978-5-7038-3026-0.
- Дриц М. Е., Будберг П. Б., Бурханов Г. С., Дриц А. М., Пановко В. М. Свойства элементов. Справочник / Под общ. ред. проф. М. Е. Дрица. — М.: Металлургия, 1985. — 672 с.
- Еремин Е. Н. Основы химической термодинамики. — 2-е изд. — М.: Высшая школа, 1978. — 392 с.
- Жданов Л. С., Жданов Г. Л. Физика для средних специальных учебных заведений. — 4-е изд., испр. — М.: Наука, 1984. — 512 с.
- Иванова Т. Е. Химическая термодинамика и ее применение в нефтегазовом деле. — Тюмень: ТюмГНГУ, 2014. — 146 с. — ISBN 978-5-9961-0925-8.
- Мейер К. Физико-химическая кристаллография. — Пер. с нем. О. П. Никитиной. — Под ред. Е. Д. Щукина и Б. Д. Сумма. — М.: Металлургия, 1972. — 480 с.
- Леонова В. Ф. Термодинамика. — М.: Высшая школа, 1968. — 159 с.
- Мякишев Г. Я., Синяков А. З. Физика. Молекулярная физика. Термодинамика. 10 класс. Профильный уровень. — 12-е изд., стереотип.. — М.: Дрофа, 2010. — 349 с. — ISBN 978-5-358-08873-3.
- Мюнстер А. Химическая термодинамика. — М.: Мир, 1971. — 296 с.
- Новиков И. И. Термодинамика. — М.: Машиностроение, 1984. — 592 с.
- Раковский А. В. Курс физической химии. — М.: Госхимиздат, 1939. — 544 с.
- Романюк В. Н., Томкунас Е. В., Баук И. В., Тарасевич Л. В. Лабораторные работы (практикум) по дисциплине «Техническая термодинамика» для студентов теплоэнергетических специальностей. В 4-х частях. Часть 2. Реальный газ. — Минск: БелНТУ, 2003. — 104 с.
- Термодинамика. Основные понятия. Терминология. Буквенные обозначения величин / Отв. ред. И. И. Новиков. — АН СССР. Комитет научно-технической терминологии. Сборник определений. Вып. 103. — М.: Наука, 1984. — 40 с.
- Техническая термодинамика / Под ред. проф. Э. И. Гуйго. — 2-е изд. — Л.: Изд-во Ленингр. ун-та, 1984. — 296 с.
- Фёдоров П. И. Тройная точка // Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — С. 12.
- Хачкурузов Г. А. Основы общей и химической термодинамики. — М.: Высшая школа, 1979. — 268 с.
- Хейвуд Р. Термодинамика равновесных процессов. Руководство для инженеров и научных работников. — М.: Мир, 1983. — 493 с.
- Химическая энциклопедия / Гл. ред. Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — 783 с. — ISBN 5-85270-310-9.
- Эйзенберг Д., Кауцман В. Структура и свойства воды. — Л.: Гидрометеоиздат, 1975. — 280 с.
