Гликолиз
Глико́лиз, или путь Эмбдена — Мейергофа — Парнаса
- Глюкоза + 2.
Общий обзор

Распад шести
Энергетическую выгоду даёт второй этап гликолиза, сопряжёный с образованием АТФ. Каждая из двух молекул глицеральдегид-3-фосфата окисляется и фосфорилируется фосфорной кислотой (а не АТФ), образуя
Таким образом, гликолиз включает в себя химические перестройки следующего типа:
- расщепление шестиуглеродного скелета глюкозы на два трёхуглеродных пирувата;
- фосфорилирование АДФ до АТФ, осуществляемое при отрыве фосфата от соединений с высоким потенциалом переноса фосфата, образующихся при гликолизе (таким образом, АТФ при гликолизе образуется за счёт субстратного фосфорилирования, в отличие от окислительного фосфорилирования дыхательной цепи, где АТФ образуется за счёт переноса электронов и протонов по цепи переносчиков[6]);
- перенос иона Н+ к НАД+ с образованием восстановленного НАДН[4].
Итак, суммарное уравнение гликолиза:
- Глюкоза + 2НАД+ + 2АДФ + 2Pi → 2 пируват + 2НАДH + 2Н+ + 2АТФ + 2Н2O[2].
Значение фосфорилирования промежуточных соединений
Каждое из 9 промежуточных соединений на пути от глюкозы к пирувату содержат остатки ортофосфорной кислоты. По-видимому, фосфатные группы в этом случае выполняют следующие 3 функции:
- Поскольку в белки-переносчики для фосфорилированных сахаров, фосфорилированные промежуточные соединения, а также глюкозо-6-фосфат не могут покинуть клетку. После первоначального фосфорилирования для удержания внутри клетки фосфорилированных соединений больше не нужно дополнительной энергии, несмотря на большую разницу между внутри- и внеклеточной концентрацией этих соединений.
- Фосфатные группы необходимы для хранения метаболической энергии. Энергия, которая потенциально может быть высвобождена при гидролизе фосфоенолпируват), выступают в качестве доноров фосфорильной группы при образовании АТФ из АДФ.
- Энергия связывания фосфатных групп с активными центрами ферментов снижает энергию активации и увеличивает специфичность ферментативных реакций. Фосфатные группы АДФ, АТФ и промежуточных продуктов гликолиза образуют комплексы с ионами Mg2+. Места связывания субстрата многих ферментов специфичны к этим комплексам. Для активности большинства ферментов гликолиза необходим Mg2+[7].
Механизм
Этап 1: подготовительный этап
На подготовительном этапе гликолиза шестиуглеродная молекула глюкозы расщепляется на два триозофосфата. При этом затрачиваются две молекулы АТФ[7]. Подготовительный этап гликолиза включает 5 реакций, которые подробно описаны ниже.
Стадия 1: фосфорилирование глюкозы
В первой реакции гликолиза происходит активация молекулы глюкозы путём её фосфорилирования по шестому атому углерода (С-6) с образованием глюкозо-6-фосфата, при этом донором фосфорильной группы выступает АТФ[8]:

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Гексокиназа | Mg2+ | −16,7 |
Эта реакция катализируется ферментом гексокиназой (в клеточных условиях гексокиназа неспособна осуществлять обратную реакцию). Он относится к группе киназ — ферментов, катализирующих перенос терминальной фосфорильной группы с АТФ на акцептор — нуклеофил. В случае гексокиназы акцептором является гексоза, как правило, D-глюкоза, хотя в некоторых тканях гексокиназа также может катализировать фосфорилирование и других распространённых гексоз, например, D-фруктозы и D-маннозы[8] (подробнее см. ниже).

Как и многим другим киназам, гексокиназе для активности необходимо присутствие ионов Mg2+, поскольку собственно субстратом для этого фермента является не АТФ4-, а комплекс MgАТФ2-. Ион магния «закрывает собой» часть отрицательного заряда фосфатных групп АТФ, делая терминальный атом фосфора более доступным для нуклеофильной атаки гидроксильной группой глюкозы. При связывании с глюкозой гексокиназа значительно изменяет конфигурацию, два её домена при связывании с АТФ сближаются друг с другом на 8 Å. Такое сближение подводит связанный с ферментом АТФ ближе к молекуле глюкозы, также с ним связанной, а также блокирует вход в активный центр воды из раствора, которая в противном случае гидролизовала бы фосфоангидридные связи в молекуле АТФ. Как и другие 9 ферментов гликолиза, гексокиназа является растворимым цитозольным белком[8].
Стадия 2: изомеризация глюкозо-6-фосфата
Фермент фосфогексозоизомераза:

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Фосфогексозоизомераза, или глюкозоизомераза |
Mg2+ | 1,7 |
Механизм этой реакции включает в себя образование промежуточного енодиольного соединения. Эта реакция одинаково хорошо идёт в обоих направлениях, как и можно было предположить из её небольшого ΔG′о. Эта изомеризация играет ключевую роль для всех последующих превращений гликолиза, поскольку перестройка карбонильной и гидроксильной групп при С-1 и С-2 необходима для следующих двух стадий. Для фосфорилирования, происходящего в следующей стадии, необходимо, чтобы при С-1 карбонильная группа была перестроена в гидроксильную, а для четвёртой стадии — разрыва связи между С-3 и С-4 — необходимо наличие карбонильной группы при С-2[8].
Стадия 3: фосфорилирование фруктозо-6-фосфата
В третьей реакции гликолиза, протекающей с затратой АТФ, фермент фосфофруктокиназа-1 катализирует перенос фосфорильной группы от АТФ на фруктозо-6-фосфат с образованием фруктозо-1,6-бисфосфата[8]:

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Фосфофруктокиназа-1 | Mg2+ | −14,2 |
В клеточных условиях фосфофруктокиназа не может осуществлять эту реакцию в обратном направлении, и эта реакция является первой реакцией, продукт которой (фруктозо-1,6-бисфосфат) участвует только в дальнейших реакциях гликолиза, потому что глюкозо-6-фосфат и фруктозо-6-фосфат могут участвовать и в других[каких?] процессах[9].
У некоторых, как правило анаэробных, бактерий и
- Фруктозо-6-фосфат + PPi → фруктозо-1,6-бисфосфат + Pi, ΔG′о = −2,9 кДж/моль, реакция идёт в присутствии Mg2+[9].
В растительных клетках имеется как АТФ-зависимая фосфофруктокиназа, так и пирофосфат-зависимая фосфофруктокиназа (реакция, катализируемая последней, обратима)[10]. Пирофосфат-зависимая фосфофруктокиназа локализована в цитозоле и активируется в условиях стресса, при дефиците АТФ (например, при аноксии) и фосфорном голодании[11].
Фосфофруктокиназа-1 регулируется
Стадия 4: расщепление фруктозо-1,6-бисфосфата
Фермент фруктозо-1,6-бисфосфатальдолаза, или просто альдолаза, катализирует обратимую альдольную конденсацию. Фруктозо-1,6-бисфосфат расщепляется на два различных триозофосфата: глицеральдегид-3-фосфат (альдозу) и дигидроксиацетонфосфат (кетозу)[9]:

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Альдолаза | 23,8 |
Существуют 2 класса альдолаз. Альдолазы класса I имеются у
Хотя
Стадия 5: изомеризация триозофосфатов
Лишь один из двух продуктов альдолазной реакции — глицеральдегид-3-фосфат — может участвовать в дальнейших превращениях гликолиза. Другой продукт — дигидроксиацетонфосфат — быстро и обратимо переводится в глицеральдегид-3-фосфат ферментом триозофосфатизомеразой[англ.][12]:

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Триозофосфатизомераза | 7,5 |
Механизм этой реакции схож с механизмом реакции, катализируемой фосфогексозоизомеразой на стадии 2. Таким образом, обе «половины» глюкозы превращаются в глицеральдегид-3-фосфат[13]. Эта реакция завершает подготовительный этап гликолиза. К его концу молекула глюкозы, фосфорилированная по С-1 и С-6, расщепляется на две молекулы глицеральдегид-3-фосфата[13].
Этап 2: синтез АТФ
Второй этап гликолиза содержит стадии, в которых часть химической энергии молекулы глюкозы запасается в виде АТФ за счёт субстратного фосфорилирования АДФ, а также образования НАДH. Две молекулы глицеральдегид-3-фосфата, образовавшиеся в ходе подготовительного этапа гликолиза, во втором этапе подвергаются одинаковым превращениям. В конечном счёте каждая из них переводится в пируват, при этом образуется 4 молекулы АТФ. Однако суммарный выход АТФ в гликолизе составляет 2 молекулы, так как 2 молекулы АТФ расходуются в подготовительном этапе[13].
Стадия 6: окисление глицеральдегид-3-фосфата
В первой реакции второго этапа гликолиза молекула глицеральдегид-3-фосфата окисляется и фосфорилируется в :

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Глицеральдегид-3-фосфатдегидрогеназа | 6,3 |
Это первая из двух энергозапасающих реакций, продукты которых в дальнейшем участвуют в образовании АТФ. Альдегидная группа глицеральдегид-3-фосфата окисляется, но не до свободной
В ходе этой реакции глицеральдегид-3-фосфат
Количество NAD+ в клетке (< 10−5 М) гораздо меньше, чем количество глюкозы, расщеплямой за несколько минут. Если NADH, образующийся на этой стадии гликолиза, не будет постоянно расходоваться (то есть окисляться), то гликолиз останавливается[15].
Стадия 7: перенос фосфатной группы с 1,3-бисфосфоглицерата на АДФ
Фермент

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Фосфоглицераткиназа | Mg2+ | −18,5 |
Этот фермент получил своё название за обратную реакцию, при которой происходит перенос фосфатной группы с АТФ на
.Стадии 6 и 7 гликолиза с энергетической точки зрения рассматриваются вместе[
- Глицеральдегид-3-фосфат + ADP + Pi + NAD+ ⇌ 3-фосфоглицерат + ATP + NADH + Н+, ΔG′о = −12,2 кДж/моль[16].
Поэтому стадии 6 и 7 вместе составляют экзергонический процесс. Обе эти реакции обратимы при клеточных условиях, и составляемый ими процесс обеспечивает запасание энергии, образовавшейся при окислении альдегидной группы до карбоксильной, в форме АТФ при его образовании из АДФ и фосфорной кислоты. Образование АТФ при переносе фосфорильной группы с субстрата (в данном случае —
Стадия 8: превращение 3-фосфоглицерата в 2-фосфоглицерат
Фермент

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Фосфоглицератмутаза | Mg2+ | 4,4 |
Реакция осуществляется в два этапа. Вначале фосфорильная группа, связанная с остатком
Стадия 9: дегидратация 2-фосфоглицерата
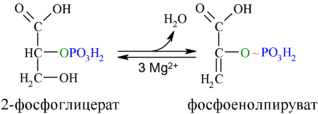
Во второй реакции гликолиза, в которой образуется соединение с более высоким потенциалом для перенесения фосфата (первой была стадия 6), фермент енолаза катализирует обратимое элиминирование воды (дегидратацию) из молекулы 2-фосфоглицерата, в результате которого образуется фосфоенолпировиноградная кислота (ФЕП)[18]:
| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Енолаза | Mg2+ | 7,5 |
Механизм реакции, катализируемой енолазой, включает стабилизацию промежуточного продукта ионами Mg2+. В ходе этой реакции соединение с относительно низким потенциалом для транспорта фосфата (ΔG′о при гликолизе 2-фосфоглицерата составляет −17,6 кДж/моль) в соединение с высоким потенциалом для транспорта фосфата (ΔG′о при гликолизе ФЕП составляет −61,9 кДж/моль)[18].
Стадия 10: перенос фосфата с ФЕП на АДФ
В последней реакции гликолиза происходит перенос фосфорильной группы с фосфоенолпирувата на АДФ, катализируемый пируваткиназой, для работы которой необходимы ионы К+ и Mg2+ или Mn2+[18]:

| Фермент | Кофактор | Изменение свободной энергии (ΔG′о, кДж/моль) |
| Пируваткиназа | К+, Mg2+/Mn2+ |
−31,4 |
Таким образом, эта реакция представляет собой субстратное фосфорилирование. Её продукт — пируват — вначале образуется в енольной форме, которая затем быстро таутомеризуется в кето-форму, которая преобладает при pH = 7 (то есть в клеточных условиях)[18].
Суммарно эта реакция имеет большое отрицательное изменение свободной энергии из-за спонтанной конверсии енольной формы пирувата в кето-форму. Около половины энергии, выделившейся при гидролизе ФЕП (ΔG′о = −30,5 кДж/моль), запасается при образовании фосфоангидридной связи в АТФ (ΔG′о = −30,5 кДж/моль), а остальная энергия (-31,4 кДж/моль) составляет мощную движущую силу для направления этой реакции в сторону образования АТФ[18].
Энергетика
С энергетической точки зрения в гликолизе можно выделить 2 процесса:
1) Превращение глюкозы в пируват — энергетически выгодный процесс:
- Глюкоза + 2NAD+ → 2 пируват + 2NADH + 2Н+, ΔG′1 = −146 кДж/моль[7];
2) Образование ATP из ADP и 2Pi — энергетически невыгодный процесс:
- 2ADP + 2Pi → 2ATP + 2Н2O, ΔG′2 = 2(30,5 кДж/моль) = 61,0 кДж/моль[7];
Общее изменение энергии Гиббса при гликолизе ΔG′s составляет:
- ΔG′s = ΔG′1 + ΔG′2 = −146 кДж/моль + 61 кДж/моль = −85 кДж/моль[7].
Поэтому при нормальных условиях, а также клеточных условиях (отличных от нормальных) гликолиз является в значительной мере необратимым процессом благодаря значительному уменьшению свободной энергии системы[7].

Из представленной выше диаграммы видно, что только три реакции (1, 3 и 10) протекают с высоким изменением свободной энергии, причём
Гликолиз других углеводов
Многие углеводы, отличные от глюкозы, также разрушаются по пути гликолиза, но после того, как они будут переведены в одно из промежуточных соединений гликолиза[20].
Гликоген и крахмал

Полимеры глюкозы
- Глюкозо-1-фосфат ⇌ глюкозо-6-фосфат.
Механизм действия этого фермента такой же, как у фосфоглицератмутазы. Образующийся в ходе этой реакции глюкозо-6-фосфат может далее быть задействован в гликолизе или пентозофосфатном пути[21].
Описанная выше ситуация характерна лишь для гликогена и крахмала, запасённых внутри клетки. Фосфоролиз гликогена и крахмала, поступающих в организм с пищей, в
Дисахариды
- Декстрин (полисахарид) + nH2O → n D-глюкоза (декстриназа);
- Мальтоза + H2O → 2 D-глюкоза (мальтаза);
- Лактоза + H2O → D-галактоза + D-глюкоза (лактаза);
- Сахароза + H2O → D-фруктоза + D-глюкоза (сахараза);
- Трегалоза + H2O → 2 D-глюкоза (трегалаза)[21].
Образующиеся моносахариды активно транспортируются в эпителиальные клетки, затем попадают в кровь и разносятся к различных тканям, где фосфорилируются и вовлекаются в гликолиз[21].
Другие моносахариды
Фруктоза
У большинства организмов гексозы, отличные от глюкозы, вовлекаются в гликолиз после преобразования в фосфорилированное производное. Гликолитическое расщепление фруктозы называется
- Фруктоза + ATP → фруктозо-6-фосфат + ADP (реакция идёт в присутствии Mg2+)[23].
Такой путь является основным механизмом вовлечения фруктозы в гликолиз в
- Фруктоза + ATP → фруктозо-1-фосфат + ADP (реакция идёт в присутствии Mg2+).
Далее фруктозо-1-фосфат расщепляется на глицеральдегид и дигидроксиацетонфосфат ферментом фруктозо-1-фосфатальдолазой. Далее дигидроксиацетонфосфат превращается в глицеральдегид-3-фосфат гликолитическим ферментом триозофосфатизомеразой, а глицеральдегид фосфорилируется ATP и ферментом триозокиназой[англ.] до глицеральдегид-3-фосфата:
- Глицеральдегид + ATP → Глицеральдегид-3-фосфат + ADP (реакция идёт в присутствии Mg2+).
Получившиеся 2 молекулы глицеральдегид-3-фосфата вовлекаются в гликолиз[23]. Ниже представлена схема вышеописанных процессов:

Галактоза
D-Галактоза, продукт гидролиза лактозы, из кишечника всасывается в кровь, откуда попадает в печень, где фосфорилируется галактокиназой по С-1 с затратой АТФ:
- Галактоза + ATP → галактозо-1-фосфат + ADP (реакция идёт в присутствии Mg2+).
Галактозо-1-фосфат далее эпимеризуется

Манноза

D-
- Манноза + ATP → маннозо-6-фосфат + ADP (реакция идёт в присутствии Mg2+).
Маннозо-6-фосфат далее изомеризуется ферментом фосфоманнозоизомеразой[англ.] до фруктозо-6-фосфата — промежуточного соединения гликолиза[23].
Регуляция
Регуляция гликолиза обычно осуществляется совместно с регуляцией обратного процесса — глюконеогенеза. У млекопитающих глюконеогенез протекает в основном в печени, где его функция заключается в синтезе глюкозы для перенесения к другим тканям в ситуациях, когда запасы гликогена истощены и с пищей в организм не поступает достаточного количества глюкозы. Как упоминалось выше, благодаря обратимости семи из десяти реакций гликолиза в ходе глюконеогенеза эти реакции протекают в обратном направлении и при катализе теми же ферментами, а для необратимых реакций (1, 3 и 10) используются обходные пути. Эти обходные реакции также необратимы. Так, при глюконеогенезе пируват переходит в фосфоенолпируват через промежуточную стадию образования оксалоацетата при катализе пируваткарбоксилазой[англ.], превращающей пируват в оксалоацетат, и фосфоенолпируваткарбоксиназой[англ.], переводящей оксалоацетат в фосфоенолпируват (обходной путь для десятой стадии). Обходная реакция для третьей стадии — превращение фруктозо-1,6-бисфосфата во фруктозо-6-фосфат ферментом фруктозо-1,6-бисфосфатазой, а для первой стадии — превращение глюкозо-6-фосфата в глюкозу глюкозо-6-фосфатазой[24].
Регуляция гексокиназы

Гексокиназа, катализирующая фосфорилирование глюкозы на стадии 1, в организме человека представлена четырьмя изоформами (I—IV). Они кодируются разными генами[какими?], но катализируют одну и ту же реакцию. В миоцитах преобладает гексокиназа II, имеющая высокое сродство к глюкозе, — её полунасыщение наступает при 0,1 мМ глюкозы. Поскольку в миоцит глюкоза попадает из крови, где концентрация глюкозы составляет 4—5 мМ, то внутри клетки поддерживается концентрация глюкозы, достаточная для насыщения гексокиназы II, и этот фермент работает в полную силу. Мышечные гексокиназы I и II аллостерически ингибируются их продуктом, глюкозо-6-фосфатом, так что при повышении внутриклеточной концентрации глюкозо-6-фосфата выше нормального уровня происходит временное обратимое подавление активности этих ферментов. Таким образом скорость образования глюкозо-6-фосфата находится в балансе со скоростью его расщепления[25].
Изоформы гексокиназы играют различные роли в углеводном метаболизме печени и мышц: в мышцах глюкоза потребляется для получения энергии, а печень поддерживает концентрацию глюкозы в крови, потребляя глюкозу или образуя её путём глюконеогенеза в зависимости от концентрации. В печени преобладает гексокиназа IV (глюкокиназа), которая отличается от мышечных гексокиназ I—III в трёх важных аспектах. Во-первых, концентрация глюкозы, при которой происходит полунасыщение гексокиназы IV, составляет около 10 мМ, что выше обычной концентрации глюкозы в крови. Быстрое выравнивание концентраций глюкозы в
Гексокиназа IV и глюкозо-6-фосфатаза также регулируются на уровне транскрипции (подробнее о транскрипционной регуляции см. ниже)[27].
Регуляция фосфофруктокиназы-1

Как уже отмечалось, глюкозо-6-фосфат может вовлекаться как в гликолиз, так и в другие процессы, в том числе в синтез гликогена и пентозофосфатный путь. Метаболически необратимая реакция, катализируемая фосфофруктокиназой-1 (PFK-1) является этапом, строго закрепляющим участие данной молекулы глюкозы только в гликолизе. Кроме субстрат-связывающих сайтов, этот сложно устроенный фермент имеет несколько регуляторных сайтов, с которыми связываются аллостерические активаторы или ингибиторы[27].
ATP является не только субстратом для PFK-1, но и конечным продуктом гликолиза. Когда высокий уровень ATP в клетке сигнализирует о том, что образование ATP превосходит его потребление, ATP связывается с PFK-1 в особом аллостерическом сайте и снижает сродство этого фермента к субстрату —
Реакции, катализируемой PFK-1, в гликолизе соответствует реакция глюконеогенеза, при которой фруктозо-1,6-бисфосфат переводится во фруктозо-6-фосфат. Эта реакция катализируется ферментом фруктозобисфосфатазой-1 (FBPаза-1). FBPаза-1 строго подавляется аллостерическим связыванием АМФ, так что когда клеточные запасы АТФ невелики, а уровень
Таким образом, противоположные этапы гликолиза и глюконеогенеза, катализируемые PFK-1 и FBPазой-1 соответственно, регулируются координированно и реципрокно (то есть обратно). Вообще, при достаточных концентрациях
Фруктозо-2,6-бисфосфат как регулятор
Особая роль печени в поддержании постоянного уровня глюкозы в крови требует дополнительных регуляторных механизмов, координирующих образование и потребление глюкозы. Когда уровень глюкозы в крови понижается,
Быстрая гормональная регуляция гликолиза и глюконеогенеза опосредована фруктозо-2,6-бисфосфатом — аллостерическим регулятором ферментов PFK-1 и FBPазы-1. Когда фруктозо-2,6-бисфосфат связывается с особым аллостерическим сайтом на PFK-1, он увеличивает сродство фермента к его субстрату —

Клеточная концентрация аллостерического регулятора фруктозо-2,6-бисфосфата складывается из относительных скоростей его образования и разрушения. Он образуется при фосфорилировании фруктозо-6-фосфата ферментом фосфофруктокиназой-2 (PFK-2), а разрушается фруктозо-2,6-бисфосфатазой (FBPазой-2). PFK-2 и FBPаза-2 представляют собой две различные ферментные активности одного и того же бифункционального белка. Баланс этих активностей в печени, определяющих клеточный уровень фруктозо-2,6-бисфосфата, регулируется глюкагоном и инсулином[32].
Глюкагон стимулирует аденилатциклазу печени к синтезу 3',5'-
Ксилулозо-5-фосфат как регулятор

Действие другого регуляторного механизма также основано на регуляции уровня фруктозо-2,6-бисфосфата. В печени млекопитающих ксилулозо-5-фосфат, продукт пентозофосфатного пути, также задействован в увеличении темпов гликолиза после потребления богатой углеводами пищи. Уровень ксилулозо-5-фосфата в клетке увеличивается, когда глюкоза, поступающая в печень, превращается в глюкозо-6-фосфат и далее участвует как в гликолизе, так и пентозофосфатном пути. Ксилулозо-5-фосфат активирует фосфопротеинфосфатазу 2А (
Регуляция пируваткиназы

У позвоночных имеется по меньшей мере 3 изозима пируваткиназы, которые различаются местонахождением в тканях и ответом на воздействия модуляторов. Высокая концентрация ATP, ацетил-CoA, длинных жирных кислот (признаки достаточной энергетической обеспеченности) аллостерически подавляют все изозимы пируваткиназы. Пируваткиназа печени (L-форма), но не мышц (M-форма), также регулируется фосфорилированием. Когда низкий уровень глюкозы в крови приводит к выбросу глюкагона, cAMP-зависимая протеинкиназа фосфорилирует L-изозим пируваткиназы, инактивируя его. Это замедляет использование глюкозы в печени как источника энергии и направляет её на экспорт в мозг и другие органы. В мышцах эффект повышения концентрации cAMP строго противоположный. В ответ на воздействие адреналина cAMP активирует распад гликогена и гликолиз[33].
Транскрипционный контроль
Большая часть вышеописанных регуляторных путей опосредована быстрыми, легко обратимыми процессами: аллостерическим эффектом, фосфорилированием фермента или связыванием с регуляторным белком. Однако существуют и механизмы регуляции, основанные на изменении количества молекул фермента в клетке за счёт изменений в балансе синтеза и разрушения фермента. Эти механизмы регулируются на уровне транскрипции соответствующего фермента[34].
Под влиянием инсулина находится транскрипция более чем 150 человеческих генов. В их числе гены, участвующие в гликолизе и его регуляции, а именно кодирующие гексокиназы II и IV, PFK-1, пируваткиназу, PFK-2/FBPазу-2[34].
Одним из
Модификации
В гликолизе может протекать дополнительная реакция, превращающая 1,3-бисфосфоглицерат в 2,3-бисфосфоглицерат; эта реакция катализируется ферментом бисфосфоглицератмутазой. 2,3-Бисфосфоглицерат может возвращаться в гликолиз под воздействием фермента 2,3-бисфосфоглицератфосфатазы, которая превращает его в

Некоторые модификации гликолиза обнаружены у бактерий. В частности, когда окисление глицеральдегид-3-фосфата на стадии 6 глицеральдегид-3-фосфатдегидрогеназой ограничено низким содержанием фосфата в среде, у
Наконец, у анаэробных бактерий существуют дополнительные пути разложения углеводов. В частности, бактерии, предпочитающие пентозы в качестве субстрата, превращают пентозы и гексозы в ксилулозо-5-фосфат, который далее расщепляется фосфокетолазой[англ.][37].
Кроме того, у некоторых
.Распространение и физиологическое значение
Гликолиз является универсальным, хотя и не единственным, путём катаболизма глюкозы и активно используется как
Как отмечалось выше, в аэробных условиях пируват после гликолиза образует ацетил-CoA и вовлекается в цикл Кребса. Две молекулы НАДH, образующиеся при гликолизе в цитозоле, в этих условиях вновь окисляются до НАД+, отдавая свои электроны в электроно-транспортную цепь (ЭТЦ), которая у эукариот находится в митохондриях. По ЭТЦ эти электроны переходят от одного переносчика к другому, пока не дойдут до конечного акцептора электронов — кислорода:
- 2НАДH + 2Н+ + O2 → 2НАД+ + 2Н2O.
Перенос электронов от НАДH к O2 в митохондриях обеспечивает энергию для синтеза АТФ путём окислительного фосфорилирования[18].
В анаэробных условиях пируват подвергается дальнейшим превращениям, обеспечивая регенерацию НАД+ и других предшественников биосинтеза (брожение). При этом образуются продукты брожения, такие, как, например, лактат или этанол. В этих условиях гликолиз является единственным способом получения энергии для синтеза ATP из ADP и Pi[19]. У некоторых анаэробов, как и у аэробов, функционирует ЭТЦ, однако конечным акцептором электронов служит не кислород, а отличное от него окисленное органическое или неорганическое вещество[41].
Также на анаэробный тип метаболизма переходят некоторые органы и ткани в условиях гипоксии (нехватки кислорода), например, скелетные мышцы при активной работе. В анаэробных условиях в них пируват преобразуется в лактат, который транспортируется в другие ткани (например, печень, сердечную мышцу) и там вновь превращается в пируват (цикл Кори)[42]. Помимо этого, анаэробный распад глюкозы имеет место в эритроцитах, так как в них отсутствуют митохондрии[42].

Особое физиологическое значение гликолиз имеет в
Медицинское значение

При накоплении лактата, образующегося при анаэробных условиях, в крови (например, при интенсивной и длительной работе) развивается
При многих типах
Увеличение темпов гликолиза у опухолевых клеток достигается увеличением синтеза гликолитических ферментов и инсулиннезависимых
Большая, по сравнению с нормальными тканями, зависимость опухолей от гликолиза даёт возможности для разработки
Высокая скорость гликолиза в опухолевых клетках также имеет значение для диагностики раковых заболеваний. Относительная скорость потребления глюкозы тканью в некоторых случаях может помочь установить нахождение опухоли. При
Эволюция
Роль гликолиза и в брожении, и в дыхании имеет
История изучения

Гликолиз стал первым тщательно описанным метаболическим путём, и по сей день, возможно, остаётся наиболее изученным. После открытия спиртового брожения в экстрактах клеток

Понимание того, что именно фосфорилированные гексозы являются промежуточными соединениями гликолиза, пришло не сразу и по счастливой случайности. В 1906 году
См. также
Примечания
- ↑ 1 2 Нетрусов, Котова, 2012, с. 123.
- ↑ 1 2 Nelson, Cox, 2008, p. 528, 530.
- ↑ 1 2 Campbell, 2011, p. 179.
- ↑ 1 2 3 Nelson, Cox, 2008, p. 530.
- ↑ Nelson, Cox, 2008, p. 528—530.
- ↑ Северин, 2011, с. 264.
- ↑ 1 2 3 4 5 6 7 Nelson, Cox, 2008, p. 531.
- ↑ 1 2 3 4 5 6 7 Nelson, Cox, 2008, p. 532.
- ↑ 1 2 3 4 Nelson, Cox, 2008, p. 533.
- ↑ Plants in action / The glycolytic pathway. Дата обращения: 18 апреля 2019. Архивировано из оригинала 20 марта 2018 года.
- ↑ William C. Plaxton. Metabolic flexibility helps plants to survive stress. Дата обращения: 15 августа 2014. Архивировано 25 февраля 2015 года.
- ↑ 1 2 3 Nelson, Cox, 2008, p. 534.
- ↑ 1 2 3 4 Nelson, Cox, 2008, p. 535.
- ↑ 1 2 Nelson, Cox, 2008, p. 535—536.
- ↑ 1 2 Nelson, Cox, 2008, p. 536.
- ↑ 1 2 3 4 Nelson, Cox, 2008, p. 537.
- ↑ Nelson, Cox, 2008, p. 537—538.
- ↑ 1 2 3 4 5 6 Nelson, Cox, 2008, p. 538.
- ↑ 1 2 Кольман, Рём, 2012, с. 152.
- ↑ 1 2 Nelson, Cox, 2008, p. 543.
- ↑ 1 2 3 4 Nelson, Cox, 2008, p. 544.
- ↑ Katz N., Jungermann K. Autoregulatory shift from fructolysis to lactate gluconeogenisis in rat hepatocyte suspensions. The problem of metabolic zonation of liver parenchyma. (нем.) // Hoppe-Seyler's Zeitschrift fur physiologische Chemie. — 1976. — Vol. 357, № 3. — P. 359—375. — PMID 955564.
- ↑ 1 2 3 4 Nelson, Cox, 2008, p. 545.
- ↑ Nelson, Cox, 2008, p. 582—583.
- ↑ Nelson, Cox, 2008, p. 583—584.
- ↑ Nelson, Cox, 2008, p. 584—585.
- ↑ 1 2 Nelson, Cox, 2008, p. 585.
- ↑ 1 2 3 Nelson, Cox, 2008, p. 586.
- ↑ Nelson, Cox, 2008, p. 586—587.
- ↑ Nelson, Cox, 2008, p. 587.
- ↑ Nelson, Cox, 2008, p. 587—588.
- ↑ 1 2 3 Nelson, Cox, 2008, p. 588.
- ↑ Nelson, Cox, 2008, p. 588—589.
- ↑ 1 2 Nelson, Cox, 2008, p. 590.
- ↑ Nelson, Cox, 2008, p. 591—592.
- ↑ Северин, 2011, с. 269—270.
- ↑ 1 2 Современная микробиология / Под ред. Й. Ленгелера, Г. Древса, Г. Шлегеля. — М.: Мир, 2005. — Т. 1. — С. 267. — 654 с.
- ↑ 5 октября 2015 года.
- ↑ Северин, 2011, с. 270.
- ↑ 1 2 Nelson, Cox, 2008, p. 528.
- ↑ Нетрусов, Котова, 2012, с. 145.
- ↑ 1 2 Северин, 2011, с. 268—267.
- ↑ 24 сентября 2015 года.
- ↑ Северин, 2011, с. 269.
- ↑ Pogatsa G. Metabolic energy metabolism in diabetes: therapeutic implications. (англ.) // Coronary artery disease. — 2001. — Vol. 12 Suppl 1. — P. 29—33. — PMID 11286305.
- ↑ Diabetes - Errors of Metabolism. Дата обращения: 4 сентября 2014. Архивировано 9 июля 2010 года.
- ↑ 1 2 Nelson, Cox, 2008, p. 540.
- ↑ Nelson, Cox, 2008, p. 540—541.
- ↑ Nelson, Cox, 2008, p. 541.
- 29 августа 2009 года.
- ↑ Otto Warburg. Über die Rolle des Eisens in der Atmung des Seeigeleis nebst Bemerkungen über einige durch Eisen beschleunigte Oxydationen. // Über die Katalytischen Wirkungen der Lebendigen Substanz. — 1928. — P. 47—66.
- ↑ Парнас Яков Оскарович — статья из Большой советской энциклопедии.
- 27 октября 2019 года.
Литература
- David E. Metzler. Biochemistry: The Chemical Reactions of Living Cells.. — 2nd edition. — Academic Press, 2003. — Т. 2. — 1973 с. — ISBN 978-0-1249-2541-0.
- David L. Nelson, Michael M. Cox. Lehninger Principles of biochemistry. — Fifth edition. — New York: W. H. Freeman and company, 2008. — 1158 p. — ISBN 978-0-7167-7108-1.
- Campbell N. A., Reece J. B., Urry L. A. e. a. Biology. 9th ed. — Benjamin Cummings, 2011. — 1263 p. — ISBN 978-0-321-55823-7.
- Кольман Я., Рём К.—Г. Наглядная биохимия. — 4-е изд.. — М.: БИНОМ. Лаборатория знаний, 2012. — 469 с. — ISBN 978-5-9963-0620-6.
- Биологическая химия с упражнениями и задачами / Под ред. С. Е. Северина. — М.: Издательская группа «ГЭОТАР-Медиа», 2011. — 624 с.
- Нетрусов А. И., Котова И. Б. Микробиология. — 4-е изд., перераб. и доп.. — М.: Издательский центр «Академия», 2012. — 384 с. — ISBN 978-5-7695-7979-0.
Ссылки
- Гликолиз (англ.)